La courbe de stabilité
Dans les noyaux, les assemblages de nucléons (protons et neutrons) ne sont pas tous robustes. La stabilité dépend de l’équilibre entre la force de répulsion électrique qu’exercent entre eux les protons (chargés positivement) et la force d’attraction nucléaire qu’exercent entre eux tous les nucléons (appelée « interaction forte »). Pour atteindre cet équilibre, il est clair que les noyaux doivent posséder un certain nombre de neutrons qui apportent le supplément de force attractive indispensable à leur cohésion. La stabilité du noyau est donc liée à un problème comptable de nombre de protons et de nombre de neutrons.
Les isotopes stables se répartissent le long d’une courbe continue qui répond à plusieurs critères :
- Les petits noyaux ont une tendance à la symétrie, c’est-à-dire qu’ils ont à peu près autant de neutrons que de protons.
- Au delà de 40 nucléons, le noyau trouve un meilleur équilibre avec plus de neutrons que de protons.
- La « courbe de stabilité » répertorie 2975 isotopes, ordonnés selon leur nombre de neutrons en X et leur nombre de protons en Y.

Les isotopes qui ont une bonne répartition entre protons et neutrons sont situés dans la zone de stabilité noire : ils ne subissent aucune transformation. Les isotopes qui ont trop de protons, ou trop de neutrons, ou qui sont trop lourds (à la fois trop de protons et trop de neutrons) sont situés hors de la zone de stabilité : ils cherchent à y rentrer, ils sont instables et tôt ou tard, ils vont se transformer spontanément : on dit qu’ils sont radioactifs.
La radioactivité alpha, bêta, gamma :
Pour parvenir à la stabilité, un isotope radioactif va se désintégrer, c’est-à-dire modifier sa composition interne suivant un processus qui dépend de sa position par rapport à la zone de stabilité. Si l’isotope radioactif est juste à côté de la zone de stabilité, sa transformation donne naissance directement à un isotope stable. Par exemple, le carbone 14 radioactif se transforme en azote 14 stable. Mais si l’isotope radioactif est loin de la zone de stabilité, il génère une chaîne de filiation radioactive avant d’aboutir à un isotope stable. Par exemple, l’uranium 238 se transforme en thorium 234, lui-même radioactif, et ainsi de suite… Le noyau va subir 14 transformations successives jusqu’à aboutir au plomb 206 stable.
Le rayonnement bêta moins : Un noyau situé juste à droite de la courbe de stabilité est radioactif car il a un neutron en trop. En transformant son neutron excédentaire en proton, il va rejoindre la courbe de stabilité. Lors de la désintégration deux particules sont émises : l’électron pour l’équilibre des charges électriques, et l’antineutrino* pour la conservation de l’énergie. L’électron éjecté est un rayonnement appelé bêta moins :
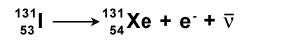
Le rayonnement bêta plus : Un noyau situé juste à gauche de la courbe de stabilité est radioactif car il a un proton en trop. En transformant son proton excédentaire en neutron, il va rejoindre la courbe de stabilité. Lors de la désintégration deux particules sont émises : le positon, particule de même masse que l’électron et de charge positive, pour l’équilibre des charges électriques, et le neutrino* pour la conservation de l’énergie. Le positon éjecté est un rayonnement appelé bêta plus :

*Particule pratiquement invisible et qui fut difficile à découvrir, le neutrino est le partenaire du positon dans le monde des particules élémentaires, de la même façon que le neutron est le partenaire du proton dans le noyau. Corpuscule élémentaire, dépourvu de charge électrique, de masse pratiquement nulle, le neutrino interagit extrêmement peu avec la matière. Tout aussi invisible, l’antineutrino, antiparticule du neutrino, est le partenaire de l’électron.
Le rayonnement alpha :
Un noyau situé au dessus de la courbe de stabilité, au delà du bismuth 209, est radioactif car trop chargé en protons et neutrons. Il va chercher à se rapprocher de la courbe de stabilité en se débarrassant de ses particules excédentaires : il éjecte en bloc 2 protons et 2 neutrons, soit un noyau d’hélium. Le noyau d’hélium éjecté est un rayonnement appelé alpha :
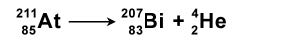
Le rayonnement gamma : Les rayonnements alpha et bêta sont très souvent accompagnés d’un autre type de rayonnement car les noyaux transformés ont encore un trop-plein d’énergie. Ils s’en libèrent en émettant un grain d’énergie sans masse de même nature que la lumière ou les rayons X appelé rayonnement gamma.